近日���,四川大學(xué)華西口腔醫(yī)學(xué)院趙行團(tuán)隊(duì)在開(kāi)發(fā)分子水凝膠進(jìn)行D-L1阻斷治療方面取得了研究進(jìn)展���。相關(guān)研究成果已發(fā)表在國(guó)際知名期刊《Advanced Functional Materials》(IF=19.924、一區(qū)top期刊)上�����。

▲ 國(guó)際知名期刊《Advanced Functional Materials》
最近研究普遍認(rèn)為免疫系統(tǒng)最初參與腫瘤的起始�、促進(jìn)和進(jìn)展, CD8+ 細(xì)胞毒性淋巴細(xì)胞 (CD8+T)是通過(guò)直接識(shí)別和分解引發(fā)抗腫瘤活性的藥物抗原呈遞腫瘤細(xì)胞���,并且參與編排了過(guò)多的系統(tǒng)性免疫反應(yīng)���。
然而,腫瘤上調(diào)程序性細(xì)胞死亡蛋白配體 1 (PD-L1) 的表達(dá),該配體與其特異性結(jié)合受體�,PD-1 在 CD8+ T 細(xì)胞上表達(dá);因此它逃避了 CD8+T 細(xì)胞介導(dǎo)的抗腫瘤作用免疫反應(yīng)����。
經(jīng)證實(shí),肌苷可促進(jìn)葡萄糖限制條件下 CD8+ T細(xì)胞毒性淋巴細(xì)胞 (CD8+T) 的增殖和功能����,并增強(qiáng)程序性細(xì)胞死亡蛋白配體-1 (PD-L1) 阻斷療法的療效。然而�,需要高頻率和大劑量的肌苷和抗 PD-L1 抗體 (aPDL1) 的全身給藥,這不可避免地會(huì)降低生物利用度并導(dǎo)致嚴(yán)重的免疫學(xué)副作用����。
因此,開(kāi)發(fā)一種藥物遞送系統(tǒng)以實(shí)現(xiàn)肌苷和aPDL1的梯度釋放用于局部免疫治療至關(guān)重要�。
在本研究中,作者成功開(kāi)發(fā)了一種基于肌苷的超分子水凝膠肌苷-苯二硼酸-異鳥(niǎo)苷 (IPBisoG)�����。體外和體內(nèi)研究都表明���,具有生物相容性和可生物降解性的 IPBisoG 水凝膠具有出色的穩(wěn)定性和自愈性能。此外��,IPBisoG 水凝膠可實(shí)現(xiàn)肌苷和 aPDL1 的逐漸和順序釋放。增強(qiáng) CD8+T 細(xì)胞增殖和功能的肌苷與腫瘤微環(huán)境中免疫抑制通路的阻斷劑 aPDL1 一起����,可高度增強(qiáng) PD-L1 阻斷治療的體內(nèi)療效。IPBisoG 水凝膠的使用也被證明可以觸發(fā)全身免疫反應(yīng)���。
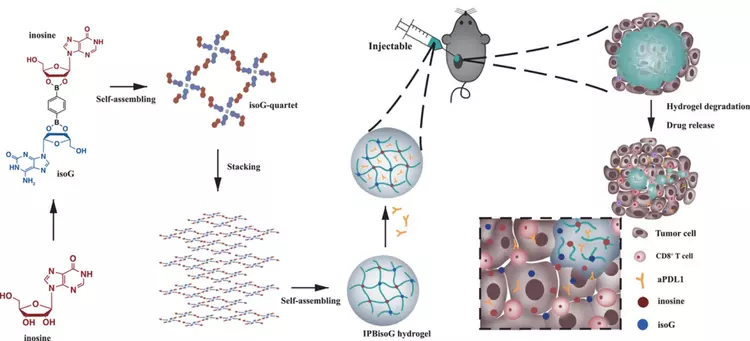
▲ IPBisoG 水凝膠的形成示意圖及其在 PD-L1 阻斷治療中作為可注射和控釋超分子水凝膠通過(guò)瘤周注射給藥程序進(jìn)行的探索
作者將aPDL1用Cy5標(biāo)記再用IPBisoG 水凝膠進(jìn)行包裹�����,然后通過(guò)尾靜脈注射到小鼠體內(nèi)�,用以評(píng)估 IPBisoG 水凝膠對(duì)aPDL1在動(dòng)物體內(nèi)滯留性的研究��,使用動(dòng)物活體成像系統(tǒng)觀察發(fā)現(xiàn)在注射72小時(shí)后���,被IPBisoG 水凝膠包裹的IaPDL1仍有明顯的信號(hào)�����,說(shuō)明IPBisoG 水凝膠能夠延長(zhǎng)aPDL1在小鼠腫瘤部位的滯留時(shí)間����。通過(guò)分析60小時(shí)時(shí)熒光信號(hào)的強(qiáng)度,也得到了相同的結(jié)論���。
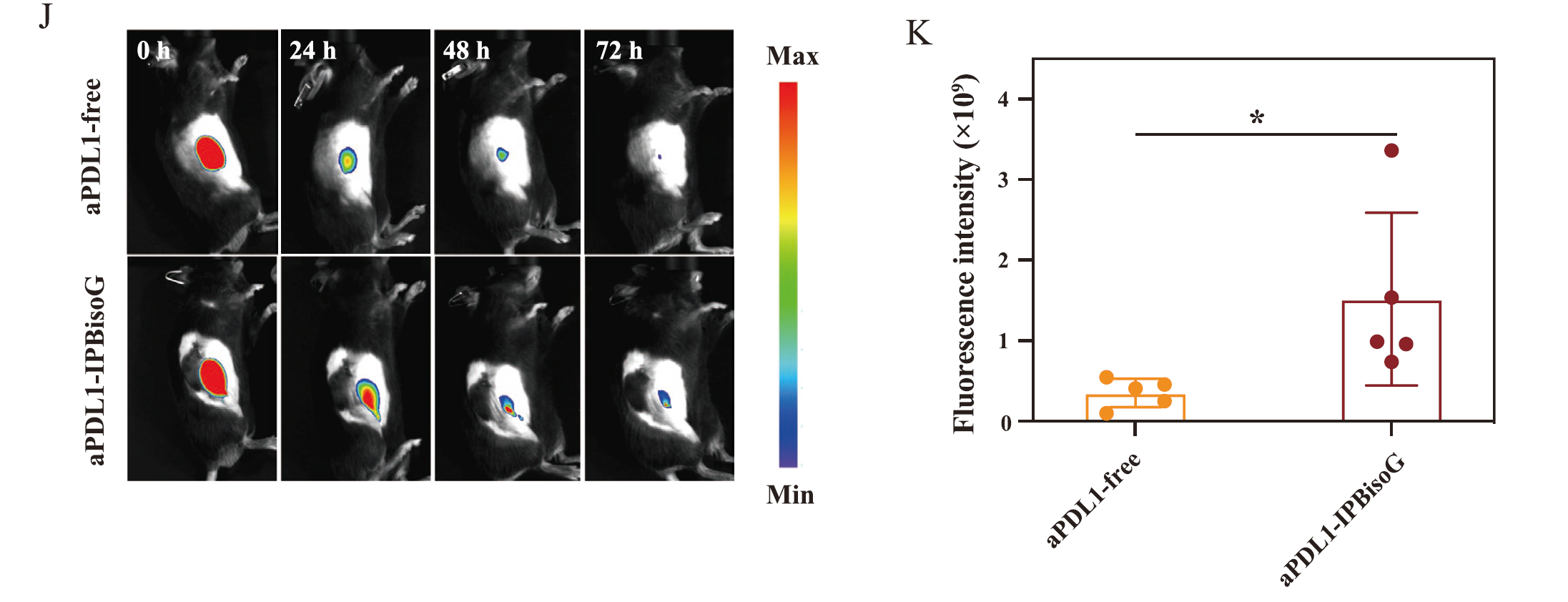
▲ IPBisoG 水凝膠對(duì)aPDL1在小鼠體內(nèi)滯留效果的研究
作者還構(gòu)建生物發(fā)光的黑色素瘤小鼠模型��,然后同樣使用動(dòng)物活體成像系統(tǒng)進(jìn)行觀察�����,結(jié)果表明IPBisoG 水凝膠+aPDL1能夠顯著抑制黑色素瘤的生長(zhǎng)����,體外解剖實(shí)驗(yàn)也能夠支持這一結(jié)論�����。
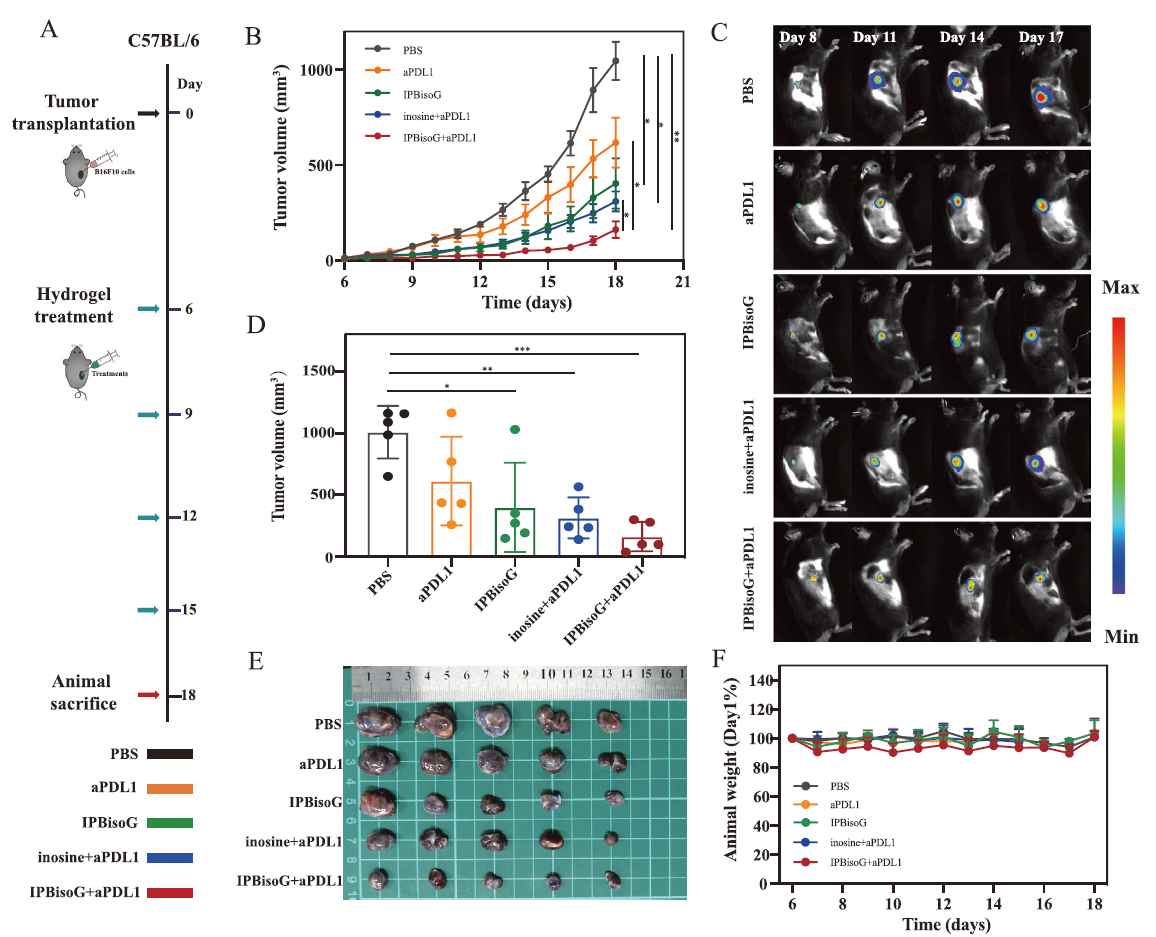
▲ IPBisoG 水凝膠對(duì)小鼠黑色素瘤治療效果的研究
博鷺騰助力科研實(shí)驗(yàn)

在IPBisoG 水凝膠對(duì)aPDL1在小鼠體內(nèi)滯留效果和對(duì)小鼠黑色素瘤治療效果的研究中�����,使用AniView系列多模式動(dòng)物活體成像系統(tǒng)進(jìn)行拍攝�。
在本研究中,研究人員設(shè)計(jì)并合成了一種新的超分子水凝膠�����,該水凝膠源自天然產(chǎn)物(肌苷和 isoG)���。IPBisoG 水凝膠可顯著增強(qiáng)腫瘤藥物滯留�����,充當(dāng)肌苷和 aPDL1釋放的儲(chǔ)庫(kù)����。此外��,局部遞送 IPBisoG 水凝膠可以有效地引發(fā)全身抗腫瘤免疫反應(yīng)�。這種新型超分子水凝膠為癌癥免疫治療提供了一種有前途的策略,并為未來(lái)其他新型藥物輸送系統(tǒng)的設(shè)計(jì)提供了一種創(chuàng)新方法���。
論文鏈接:
https://doi.org/10.1002/adfm.202204273