該論文揭示了核受體HNF4α在浸潤性黏液型肺腺癌(invasive mucinous lung adenocarcinoma��,IMA)生長和轉(zhuǎn)移過程中的作用及相關(guān)分子機制�����,并從FDA批準上市藥物庫篩選到能有效抑制IMA生長和轉(zhuǎn)移的新型HNF4α拮抗劑��,為IMA治療提供新靶點和策略����。

△ 圖1
國際權(quán)威腫瘤學雜志Cancer Research(IF=12.701)
IMA是一種惡性程度較高的肺腺癌亞型,因初期極易被誤診為肺炎�、肺結(jié)核等而耽誤治療,確診時常處于中晚期。此時手術(shù)切除可能性低���,常以放化療為主要手段�����,毒副作用大���,療效差。
近年來����,分子靶向抗腫瘤藥物在肺腺癌臨床治療中取得可喜的療效����,代表性藥物如EGFR抑制劑易瑞沙和泰瑞沙等。這類藥物具有特異性強�����、用藥量低���、毒副作用小��、人體耐受性好等優(yōu)點����,應(yīng)用前景廣泛。
但肺腺癌可細分為原位腺癌����、微浸潤腺癌、IMA����、實體型腺癌等十余種分型,具有高度的組織學和遺傳學異質(zhì)性���,必須進行個體化精準治療����。例如�����,IMA無EGFR突變卻常具KRAS突變(非KRAS G12C)����;對其而言����,EGFR抑制劑不適用���,但以KRAS突變?yōu)榘袠擞蛛y以成藥���。因此,更多新的IMA分子靶點及相應(yīng)靶向藥物亟需研發(fā)��。
核受體HNF4α在人正常肺組織中不表達�,而在約90%IMA中出現(xiàn)異常表達,可作為IMA輔助診斷標志物����。然而����,HNF4α在IMA發(fā)生發(fā)展中的作用及機制尚不清楚。
本研究中���,他們發(fā)現(xiàn)IMA細胞系及臨床樣本中表達的是由P2啟動子驅(qū)動的HNF4α�,并通過細胞水平和小鼠模型證實HNF4α依賴于其轉(zhuǎn)錄激活活性促進IMA的生長��、侵襲和遷移。
進一步研究發(fā)現(xiàn)���,HNF4α轉(zhuǎn)錄激活lncRNA BC200的表達�;而BC200作為HNF4α的下游分子���,介導(dǎo)了HNF4α促IMA生長和轉(zhuǎn)移的作用�����。在IMA細胞質(zhì)中��,BC200作為“橋梁”促進mRNA結(jié)合蛋白FMR1與腫瘤相關(guān)基因如EGFR和Twist等的mRNA的結(jié)合來調(diào)節(jié)這些mRNA的穩(wěn)定性����,從而促進IMA的生長���、侵襲和遷移����。反過來�,BC200還能通過介導(dǎo)HNF4α mRNA與FMR1的結(jié)合來增強其穩(wěn)定性,從而正反饋調(diào)控HNF4α的表達�。
基于上述發(fā)現(xiàn)�,他們還從FDA批準上市藥物庫中篩選出了HNF4α新型拮抗劑前藥霉酚酸酯(MMF)�,并通過體外及體內(nèi)實驗證實MMF的活性代謝物霉酚酸(MPA)能通過拮抗HNF4α來抑制BC200的表達和IMA生長及轉(zhuǎn)移,具備開發(fā)成IMA靶向藥的潛力����。
△ 圖2
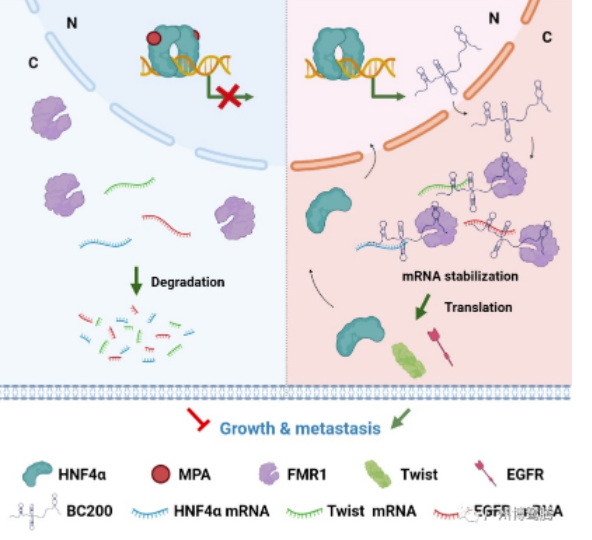
文章提出的HNF4α-BC200-FMR1反饋環(huán)在IMA生長和轉(zhuǎn)移中的作用模型
△ 圖3
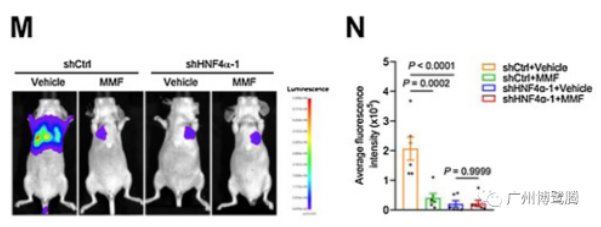
M和N分別為每組裸鼠肺內(nèi)熒光素酶表達的圖像和定量結(jié)果。
文章中���,體內(nèi)驗證MMF在IMA中的抗生長和抗轉(zhuǎn)移作用的活體成像實驗�����,使用了AniView100多模式動物活體成像系統(tǒng)進行拍攝���。
論文鏈接https://cancerres.aacrjournals.org/content/81/23/5904.abstract