急性髓系白血病(Acute Myeloid Leukemia, AML)是一組具有髓系特征的多發(fā)性異質性惡性腫瘤。通過化療����、放療、造血干細胞移植�����、支持性治療和靶向治療等方式���,可以提高患者五年總存活率�����;但是�,與其他血液腫瘤相比,AML的治療效果較差��,最常見的表現(xiàn)是緩解后復發(fā)��。因此�,對于復發(fā)和化療耐藥的患者來說,迫切需要尋找新的具有有效和可控副作用的治療藥物和技術��。
溶瘤病毒(Oncolytic Virus, OVS)是一類具有復制能力的腫瘤殺傷型病毒���,通過直接溶解感染的腫瘤細胞和間接增強宿主的抗腫瘤免疫力來介導腫瘤細胞的破壞����。其種類有:新城疫病毒(Newcastle disease virus, NDV)����、單純皰疹病毒-1(Herpes simplex virus-1, HSV-1)、呼腸孤病毒(Reovirus)和溶瘤腺病毒(Oncolytic adenovirus)等��。由于OVS優(yōu)先破壞腫瘤細胞����,而對正常細胞無害���,同時越來越多的研究證據(jù)表明,AML細胞感染溶瘤病毒會顯著增加腫瘤細胞的死亡率����,這為AML的治療提供了新的方法和思路����,已經(jīng)在多個臨床試驗中進行了安全性和可行性的探索。然而�,B淋巴細胞會對血液循環(huán)中的OVS產(chǎn)生中和抗體(Neutralizing Bntibodies、NAbs)��,從而阻止病毒的傳播�����,最終會降低病毒的治療效果���。
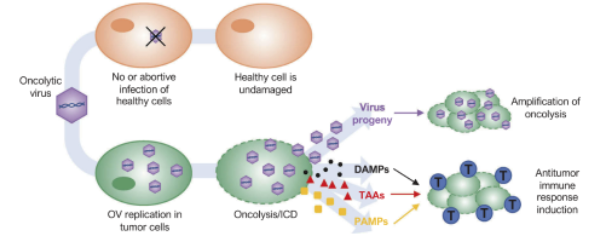
▲ OVS的雙重作用模式��,優(yōu)先靶向并殺死癌細胞����,而對正常細胞幾乎沒有有害的影響
間充質干細胞(Mesenchymal stem cells, MSCs)是一類存在于多種組織(如骨髓、臍帶血和臍帶組織�、胎盤組織、脂肪組織等)��,具有多向分化潛力的多能干細胞���。在過去的十年中����,MSCs被認為是OVS的理想載體��,其原因有:(1)����、MSCs為病毒提供了一個復制場所;(2)�、MSCs能避免被免疫系統(tǒng)清除;(3)����、MSCs確保病毒能到達腫瘤部位;(4)����、MSCs會分泌細胞因子����,增強抗腫瘤免疫反應���。然而���,攜帶溶瘤病毒的人臍帶來源的間充質干細胞(Human umbilical cord-derived MSCs, Huc-MSCs)的抗腫瘤效果及其分子機制尚不清楚。
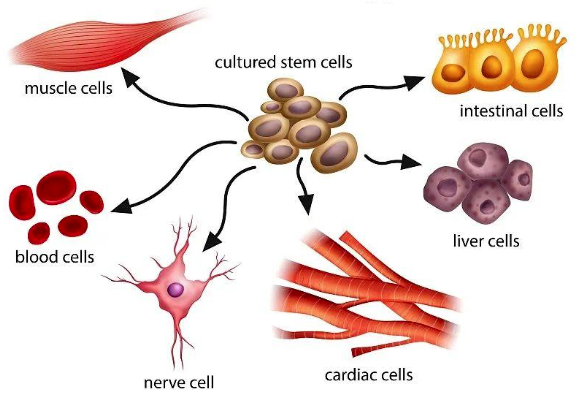
▲ 間充質干細胞的分化潛力
近日�����,貴州醫(yī)科大學成體干細胞轉化研究重點實驗室趙星和何志旭教授課題組首次報道Huc-MSCs作為呼腸孤病毒的細胞載體����,并使用博鷺騰AniView100多模式動物活體成像系統(tǒng)檢測攜帶呼腸孤病毒的Huc-MSCs和MSCs在活體內對AML的治療效果和抗腫瘤效果����。該工作有助于提升研究人員對MSCs攜帶OVS的抗腫瘤機制的理解,并可能為臨床治療AML提供新的策略��。相關成果已在國際著名期刊《International Immunopharmacology》發(fā)表���。

評價攜帶呼腸孤病毒的Huc-MSCs在體內的治療效果����。根據(jù)熒光素酶報告基因可用于體內移植的Huc-MSCs的定量,將呼腸孤病毒(Luc-MSCs-Reo)負載于Huc-MSCs���,并靜脈注射注射到AML小鼠模型內�。通過博鷺騰AniView100多模式動物活體成像系統(tǒng)進行成像�,結果顯示Huc-MSCs位置同腫瘤THP-1細胞定位相同。小鼠的Kaplan-Meier生存曲線結果表明��,接受呼腸孤病毒感染的Huc-MSCs的小鼠的中位存活時間比接受裸鼠呼腸孤病毒的小鼠顯著增加�����。這些數(shù)據(jù)證實了Huc-MSCs作為呼腸孤病毒載體具有良好的治療效果�。
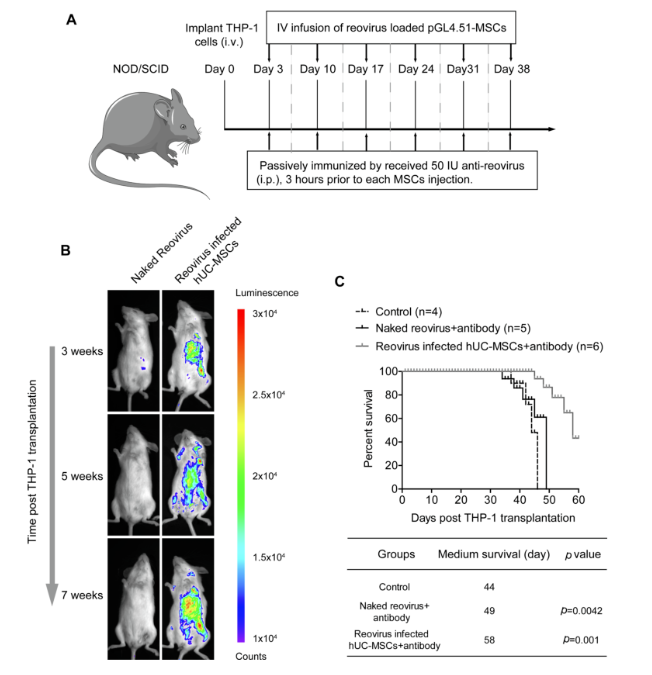
▲ 攜帶呼腸孤病毒的Huc-MSCs對AML小鼠模型的治療作用
評價攜帶呼腸孤病毒的MSCs的體內抗腫瘤效果。建立具有免疫活性的小鼠AML模型���,通過博鷺騰AniView100多模式動物活體成像系統(tǒng)進行成像�����,結果顯示標記DIR的MSCs和呼腸孤病毒感染的MSCs對C1498腫瘤具有腫瘤歸巢能力���,提示攜帶呼腸孤病毒的MSCs維持其固有的向腫瘤細胞遷移的能力���。根據(jù)各組的腫瘤體積和重量、腫瘤中的病毒RNA定量顯示����、治療后小鼠血清干擾素-γ和腫瘤壞死因子-α水平及免疫組織化學法觀察到腫瘤中CD8的表達結果,可得MSCs有效地將呼腸孤病毒運送到腫瘤部位�,并觸發(fā)小鼠的免疫反應,對腫瘤生長有明顯的抑制作用���。這些結果證實了MSCs載體能夠增強呼腸孤病毒的抗腫瘤效果�。

參考文獻:
[1] Wang X, et al. Mesenchymal stem cell carriers enhance antitumor efficacy induced by oncolytic reovirus in acute myeloid leukemia[J]. International Immunopharmacology, 2021, 94: 107437.
[2] Davola M E , et al. Oncolytic viruses: how "lytic" must they be for therapeutic efficacy?[J]. Oncoimmunology, 2019:1-7.