納米載藥系統(tǒng)
隨著納米技術(shù)的不斷發(fā)展,各種納米給藥系統(tǒng)也相繼開發(fā)出來(如脂質(zhì)體��、高分子膠束、納米凝膠和高分子藥物等)���,為進一步降低體內(nèi)游離藥物含量�、減少化療藥物的不良反應(yīng)���、提高藥物的生物利用度和治療效果等做出了突出貢獻���。然而,幾乎所有的納米載體都只是藥物轉(zhuǎn)運的輔料��,沒有治療作用���,且大量使用會因為載體代謝清除不良而導致毒性�。如何降低納米載體潛在風險或開發(fā)具有生物活性納米載體�,是一個極具吸引力的挑戰(zhàn)。
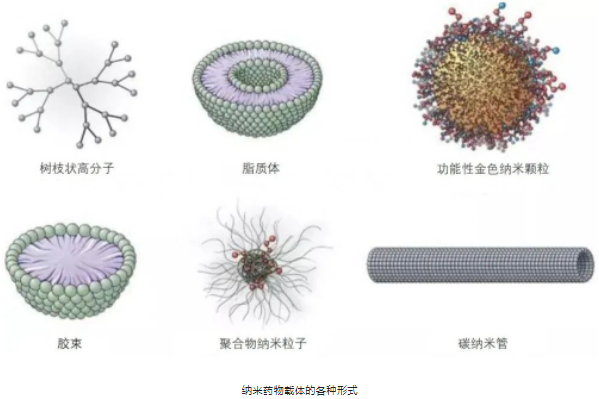
天然小分子納米載藥系統(tǒng)
天然小分子(Natural small molecules�����、NSM)具有廣泛的藥理作用。據(jù)估計�,所有小分子抗癌藥物中約有80%是天然產(chǎn)物或其衍生物,它們通常來源于活體的內(nèi)源性化學成分或代謝產(chǎn)物�����,具有良好的生物安全性�、生物穩(wěn)定性和低毒副作用等優(yōu)點,可以作為納米藥物載體(Nanomedicine-cum-carrier�����、NMC)給藥系統(tǒng)����。隨著具有自組裝性質(zhì)的NSMs相繼被發(fā)現(xiàn),NSM獨特的自組裝能力使其能夠形成不同形狀和大小的納米粒子(Nanoparticles��、NPs)����,當這些NPs作為NMC用于藥物輸送時,可以達到輔助治療和保健的作用����,從而彌補NMC藥理活性的不足��,降低納米毒性的風險��,是非常有前途的NMC�。
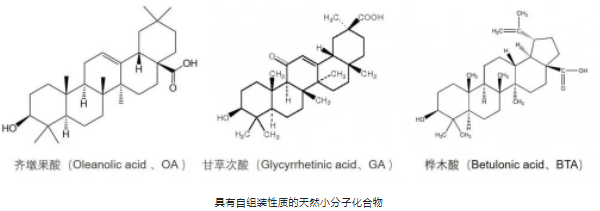
超分子共組裝
超分子共組裝方法(Supramolecular co-assembly����,由分子構(gòu)筑單元通過非共價相互作用自組裝而成)因其簡單���、綠色等優(yōu)點被廣泛應(yīng)用于構(gòu)建納米遞送載體平臺�����,納米單元在共組裝過程中保持并擁有各組成單元的生物活性���,從而獲得協(xié)同抗腫瘤、減緩化療藥物副作用和提高腫瘤治療效果���。
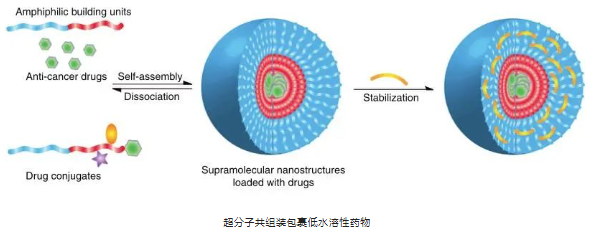
新型NMS
近日���,哈爾濱工業(yè)大學化工與化學學院食品科學與工程系楊鑫教授課題組使用天然小分子化合物齊墩果酸(Oleanolic acid、OA)、甘草次酸(Glycyrrhetinic acid���、GA)和樺木酸(Betulonic acid���、BTA),通過超分子共組裝方法設(shè)計并制造了一系列基于生物活性NSM的新型NMC�����,為共組裝納米藥物的制備和其他生物活性NSM相互作用的組裝工藝提供了參考����、為NSM的生物活性納米載藥給藥系統(tǒng)提供了范例、證明NSM對宿主具有固有的生物活性��,并且它們是很有前途的候選藥物載體�。在此基礎(chǔ)上,還為構(gòu)建用于精密治療的納米自組裝材料提供了新的視角�。相關(guān)成果已相繼發(fā)表在ACS Applied Materials & Interfaces、Biochemical Pharmacology和New Journal of Chemistry���。
文章一
具有自組裝特性的天然小分子(NSM)藥物由于其固有的生物安全性和藥理活性�,不需要復雜的結(jié)構(gòu)修飾過程����,在生物醫(yī)學領(lǐng)域應(yīng)用中具有很大的吸引力�����。然而�����,具有藥理作用的藥物載體的開發(fā)還不夠成熟�。首先并不是所有的NSM都能自組裝成具有特定形態(tài)和尺寸的藥物載體��,或具有良好的藥理活性���;其次,大量研究表明�����,構(gòu)建具有“藥理活性”的藥物載體通常需要進行化學修飾�����,這會增加復雜性(設(shè)計���、合成�����、分離和提純)和成本(產(chǎn)率低�����,原料昂貴)�,并帶來未知的生物相容性、代謝紊亂和載體誘導的毒性(多器官炎癥)等潛在問題���,嚴重限制其臨床應(yīng)用����。雖然大量的無毒納米載體不斷被開發(fā)和應(yīng)用�����,但它們都是非生物活性材料��。因此�,迫切需要開發(fā)一種有效、方便的基于NSM的納米載體制備策略�,以解決納米載體形態(tài)尺寸不合適�����、藥理活性不明顯等問題����。
本文通過超分子共組裝策略�����,首次開發(fā)出一系列具有多種藥理活性的純NSM納米載體��。具有代表性的齊墩果酸-甘草次酸納米粒子(OA-GA NPs)研究結(jié)果表明����,OA和GA具有協(xié)同作用,能顯著提高腫瘤治療效果����;可負載紫杉醇(Paclitaxel�、PTX),載藥量高達15%�,與OA-GA NPs相比,OA-GA-PTX NPs的抗腫瘤活性進一步提高�,符合臨床聯(lián)合用藥的原則�。此外���,與其他藥物載體相比����,這些NPs由于OA和GA都具有良好的保肝和抗炎活性�,在預防保健方面具有獨特的優(yōu)勢,與PTX共給藥可有效減輕PTX所致的肝損傷�����。
綜上所述���,共組裝是構(gòu)建基于NSM的“多生物活性”給藥系統(tǒng)的一種有效策略���,打破了藥理活性化合物不能直接應(yīng)用的缺點,增強了藥物載體的藥理活性����,提高了抗腫瘤療效,減緩了化療藥物的副作用和長期使用非生物活性納米載體帶來的額外毒性����。這為制備“藥理活性”納米載體提供了新的視角��,為共組裝納米藥物的制備和其他生物活性NSM相互作用的組裝工藝提供了參考����。
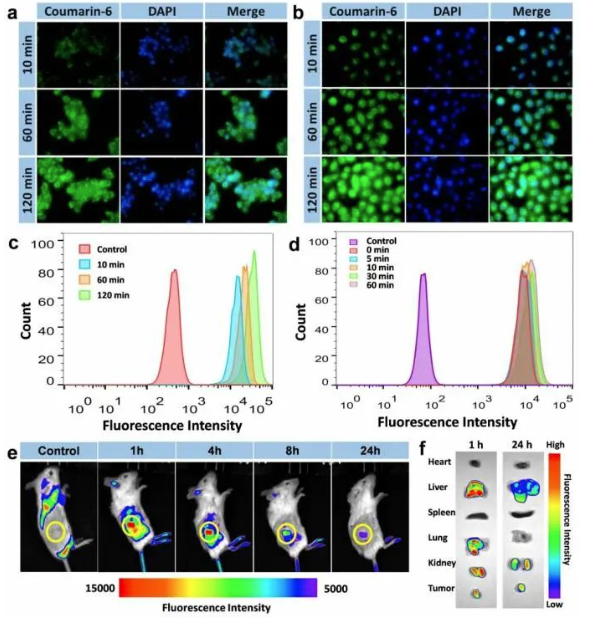
胞細攝取OA-GA-PTX NPs的能力及RhB標記的OA-GA NPs在體內(nèi)的生物分布���。a-b���、OA-GA-Ce6 NPs與4T1和MCF-7細胞孵育不同時間的代表性圖像(a表示4T1細胞,b表示MCF-7細胞)(×400)�;c、流式細胞術(shù)分析細胞吞噬OA-GA-Ce6 NPs的功能�;d、流式細胞術(shù)分析熒光染料在細胞內(nèi)的釋放情況���;e���、博鷺騰多模式動物活體成像系統(tǒng)拍攝的特定時間點NPs在腫瘤的分布;f���、注射RhB標記的OA-GA NPs后不同時間點安樂死4T1荷瘤小鼠腫瘤和正常組織的體外熒光成像。
文章二
乳腺癌是世界上發(fā)病率最高的癌癥之一��。在乳腺癌的治療中,紫杉醇(PTX)是最優(yōu)秀的天然抗癌藥之一�;然而,PTX的副作用和生物利用度低限制了其臨床應(yīng)用�����。納米制劑作為一種藥物釋放系統(tǒng)被廣泛應(yīng)用于提高藥物的生物利用度和治療活性��。最近的研究發(fā)現(xiàn)��,基于具有自組裝特性的天然小分子(NSM)納米給藥系統(tǒng)顯示出優(yōu)異的生物活性��。樺木酸(BTA)是一種天然的五環(huán)三萜羧酸����,具有良好的抗腫瘤活性,對正常細胞具有高劑量耐受性���。
本文基于NSMs的超分子共組裝納米遞送系統(tǒng)�,開發(fā)了基于BTA和PTX的超分子共組裝納米粒子(NPs)����。該共組裝納米粒子既具有納米粒子的特性,又具有NSM的活性�����。體內(nèi)外研究結(jié)果表明,這種共組裝策略綜合了納米遞送系統(tǒng)和聯(lián)合治療的優(yōu)點���,不僅可以通過BTA和PTX不同的抗腫瘤機制產(chǎn)生協(xié)同抗腫瘤作用�,而且可以通過增強通透性和滯留(EPR)效應(yīng)來實現(xiàn)精確的藥物靶向和提高PTX的生物利用度����。此外,BTA的使用提高了NPs的生物安全性�����,降低了其對正常組織器官的毒性�����。更重要的是����,通過超分子共組裝構(gòu)建藥物傳遞系統(tǒng)的方法解決了單組分自組裝形態(tài)不合適的問題,為制備具有新形貌特征的納米顆粒提供了新的思路�����,為構(gòu)建基于NSM的生物活性納米載藥給藥系統(tǒng)提供了范例�����。
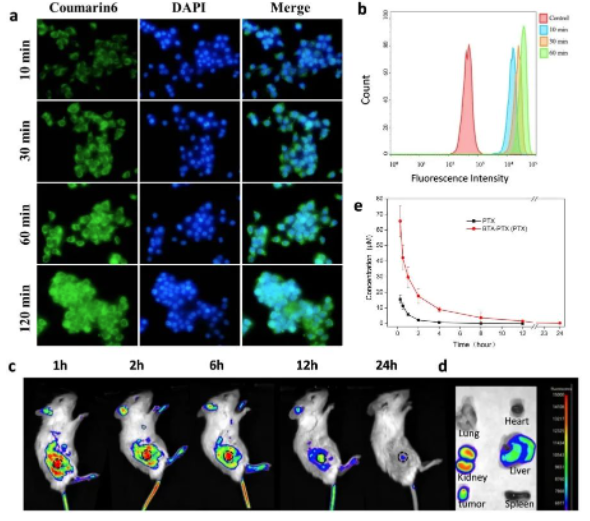
BTA-PTX NPs細胞體外攝取和體內(nèi)生物分布�����。a����、熒光倒置顯微鏡觀察4T1細胞攝取BTA-PTX NPs,攝取量隨時間增加(×400)�����;b�、流式細胞術(shù)定量研究4T1細胞攝取BTA-PTX NPs情況;c�、將熒光標記的BTA-PTX NPs經(jīng)尾靜脈注射到小鼠體內(nèi),博鷺騰多模式動物活體成像系統(tǒng)監(jiān)測NPs的腫瘤靶向性�;d、腫瘤和正常組織的體外熒光成像�����,NPs主要積聚在腎臟和腫瘤組織;e���、給藥后血藥濃度-時間曲線�����,BTA-PTX血藥濃度明顯高于PTX���。
文章三
化療一直是大多數(shù)腫瘤患者不可或缺的治療手段,但是幾乎所有化療藥物都會對肝有不同程度的損傷����,且對胃腸道還有很強的副作用。納米藥物載體系統(tǒng)的研發(fā)和應(yīng)用為腫瘤的治療開辟前所未有的新機遇�,然而載體存在潛在的毒性風險,會增加肝臟的負荷����。齊墩果酸(OA)在中國藥用植物中大量存在,作為一種重要的天然藥物����,具有抗氧化��、抗腫瘤和保肝等作用����。
為了減緩化療藥物所致的肝臟損傷��,降低納米毒性的潛在風險���,本文以齊墩果酸為組成單元,通過超分子共組裝包封紫杉醇(PTX)��,構(gòu)建了一種生物活性納米藥物載體(NMS)給藥系統(tǒng)�����。體內(nèi)外研究結(jié)果表明����,該系統(tǒng)OA和PTX維持各自獨特的生物活性單位,具有協(xié)同抗腫瘤作用����。由于OA的保肝活性,PTX引起的肝損傷明顯減少����。此外��,制備的納米藥物載藥量高����、靶向性好�、生物相容性好、體內(nèi)毒性低��,保證了腫瘤治療的有效性和機體的安全性�。這些結(jié)果證明了天然小分子(NSM)對宿主具有固有的生物活性,并且它們是很有前途的藥物載體候選���。
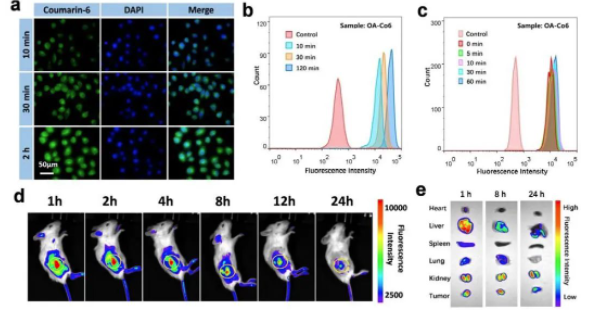
MCF-7細胞攝取OA-PTX NPs的能力及RhB標記的OA NPs在荷瘤小鼠體內(nèi)的分布�����。a����、不同孵育時間OA-Ce6 NPs與MCF-7細胞的代表性圖像(×400)�����;b、流式細胞儀分析細胞吞噬OA-CE6 NPs的情況��;c��、流式細胞術(shù)分析熒光染料在細胞內(nèi)的釋放情況���;d�����、博鷺騰多模式動物活體成像系統(tǒng)拍攝的特定時間點NPs在腫瘤的分布;e�����、注射RhB標記的OA NPs后不同時間點安樂死4T1荷瘤小鼠腫瘤和正常組織的體外熒光成像�。
文章四
用于聯(lián)合治療的多藥給藥系統(tǒng)已被認為是一種很有前途的腫瘤治療策略。光動力療法(Photodynamic therapy����、PDT)是用光敏藥物和激光活化治療腫瘤的一種精密治療方法;在光動力療法中���,氯化物e6(Chlorin e6����、Ce6)具有高效的抗癌作用,是一種應(yīng)用廣泛的光敏劑��。傳統(tǒng)化療藥物和Ce6組成的無載體純納米微球給藥系統(tǒng)(化療-光動力療法)療效顯著��,但是存在毒副作用大���,給臨床應(yīng)用帶來巨大的挑戰(zhàn)���。萜類天然小分子(NSM)具有抗癌、抗炎���、抗菌�、納米功能化等生物活性��,由于目前缺乏對NSM作為藥物載體的認識和實用性����,限制了其在生物醫(yī)學上的應(yīng)用。
為了開發(fā)基于具有抗癌活性的納米粒子和光敏藥物Ce6的腫瘤治療策略�,本文通過超分子共組裝策略,報道并開發(fā)了一系列無載體萜類天然小分子介導的共組裝光敏藥物��,用于增強和協(xié)同化療/光動力學治療。具有代表性的樺木酸修飾的BC-Ce6 NPs的研究結(jié)果表明�,組裝的納米藥物通過I型光反應(yīng)機制生成ROS;同時���,表現(xiàn)出多種良好的治療特性���,腫瘤消融率高達93.6%,實現(xiàn)了腫瘤的體內(nèi)外化療/光動力聯(lián)合治療的顯著增強和協(xié)同消融作用����。這項工作不僅突出了NSM作為新型藥物輸送平臺的潛力,而且也為構(gòu)建用于精密治療的納米自組裝材料提供了新的視角�。
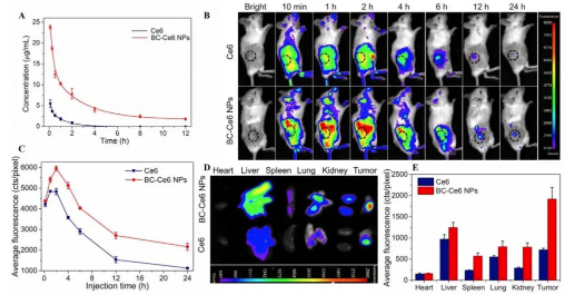
BC-Ce6 NPs在體內(nèi)的血液循環(huán)和生物分布情況。A����、靜脈注射BC-Ce6 NPs或游離Ce6后血液中Ce6的濃度-時間分布��;B�、博鷺騰多模式動物活體成像系統(tǒng)拍攝的靜脈注射4T1荷瘤小鼠BC-Ce6NPs或等效濃度Ce6后的體內(nèi)熒光圖像;C���、B內(nèi)腫瘤部位的平均熒光強度��;D���、注射24小時后采集的主要器官和腫瘤的體外熒光成像��;E��、D中從體外器官獲得的熒光強度���。
1、Wang J , Zhao H , Qiao W , et al. [J]. ACS Applied Materials & Interfaces, 2020.2�、 Wang J , Qiao W , Zhao H , et al. [J]. Biochemical Pharmacology, 2020.3、Wang J , Qiao W , Zhao H , et al. [J]. New Journal of Chemistry.4���、Cheng J , Zhao H , Wang J , et al. [J]. ACS Applied Materials & Interfaces, 2020.5�����、Lin R , Cui H . [J]. Current Opinion in Chemical Engineering, 2015, 7:75-83.